फार्मलआवेश सूत्र
किसी परमाणु पर फार्मलआवेश = परमाणु में संयोजकता इलेक्ट्रॉनों की कुल संख्या-एकाकी इलेक्ट्रॉनों की कुल-बंधो की कुल संख्या
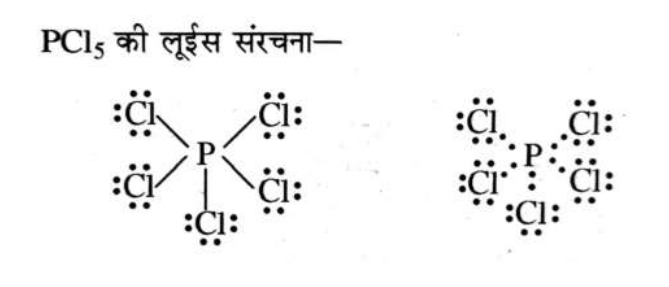
P फार्मलआवेश = 5 – 0 – 5 = 0
Cl फार्मल आवेश = 7 – 6 – 1 = 0
फॉर्मल आवेश से सम्बन्धित महत्त्वपूर्ण तथ्य
- फॉर्मल आवेश का सिद्धान्त आबंधन की शुद्ध सहसंयोजी प्रकृति पर आधारित होता है , जिसमेंआबंधित परमाणुओं के मध्य इलेक्ट्रॉनों का समान साझा होता है।
- एकउदासीनअणु में सभी परमाणुओं के फॉर्मल आवेश का योग शून्य होता है।
- किसी अणु में जब सभी बन्ध सहसंयोजी होते हैं तो उस अणु में उपस्थित सभी परमाणुओं का फॉर्मल आवेश शून्य होता है।
- किसी आयन में उपस्थित सभी परमाणुओं के फॉर्मल आवेश का योग , उस आयन पर उपस्थित आवेश के बराबर होता है।
- जब किसी अणु में उपसहसंयोजी बन्ध उपस्थित होता है तो दाता परमाणु पर फॉर्मल आवेश +1 तथा ग्राही परमाणु पर फॉर्मल आवेश -1 होता है क्योंकि उपसहसंयोजी बन्ध के बनने पर दाता परमाणु सेइलेक्ट्रॉन अभ्र ग्राही परमाणु की ओर प्रतिस्थापित होता है।