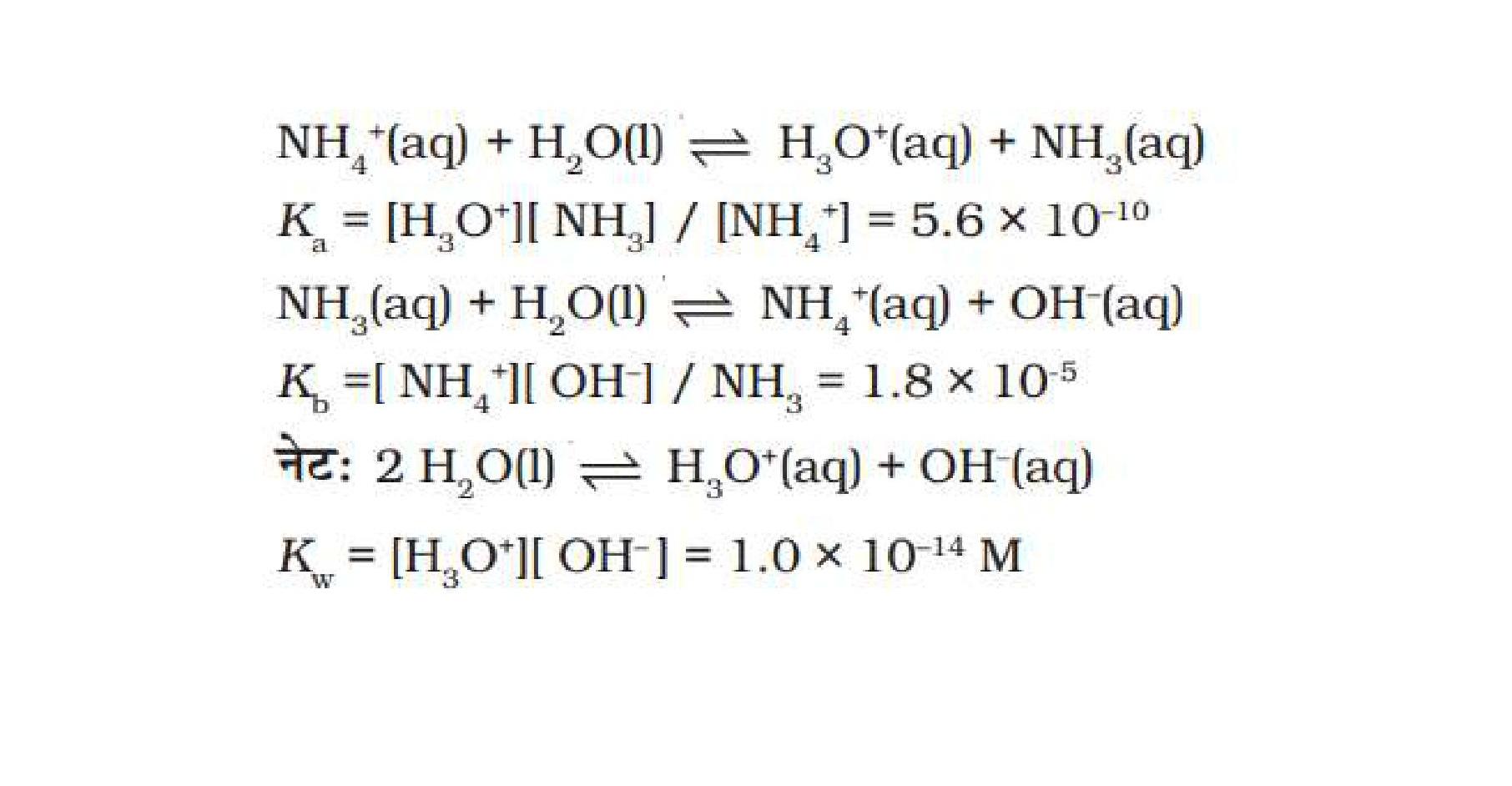अम्ल, क्षारक एवं लवण
अम्ल, क्षारक एवं लवण प्रकृति में व्यापक रूप से पाए जाते हैं। जठर रस, जिसमें हाइड्रोक्लोरिक अम्ल पाया जाता है, हमारे आमाशय द्वारा प्रचुर मात्रा (1.2-1.5 L/दिन) में स्त्रावित होताहै।
यह पाचन प्रक्रिया के लिए अति आवश्यक है। सिरके कामुख्य अवयव एसीटिक अम्ल है। नीबू एवं संतरे के रस मेंसिट्रिक अम्ल एवं एस्कार्बिक अम्ल तथा इमली में टार्टरिकअम्ल पाया जाता है। अधिकांश अम्ल स्वाद में खट्टे होते हैं,लैटिन शब्द Acidus से बना ‘एसिड’ शब्द इनके लिए प्रयुक्तहोता है, जिसका अर्थ है खट्टा। अम्ल नीले लिटमस को लालकर देते हैं तथा कुछ धतुओं से अभिक्रिया करके डाइहाइड्रोजन उत्पन करते हैं। इसी प्रकार क्षारक लाल लिटमस को नीलाकरते हैं तथा स्वाद में कड़वे और स्पर्श में साबुनी होते हैं।क्षारक का एक सामान्य उदाहरण कपड़े धोने का सोडा है,
अम्ल तथा क्षारक की आरेनियस धरणा–
आरेनियस के सिदांतानुसार अम्ल वे पदार्थ हैं, जो जल में अपघटित होकर हाइड्रोजन आयन देते हैं तथा क्षारक वे पदार्थ हैं, जो हाइड्रक्सिल आयन देते हैं। इस प्रकार जल में एक अम्ल HX का आयनन निम्नलिखित समीकरणों में से किसी एक के द्वारा प्रदर्शित किया जा सकता है– या एक मुक्त प्रोटान, अत्यधिक क्रियाशील होता है। स्वतंत्रा रूप से जलीय विलयन में इसका अस्तित्व नहीं है। यह विलायक जल अणु के आक्सीजन से बंध्ति होकर त्रिकोणीय पिरामिडी हाइड्रोनियम आयन, देता है
अम्लों एवं क्षारकों का आयनन
अधिकतर रासायनिक एवं जैविक अभिक्रियाएं जलीय माध्यम में होती हैं। इन्हें समझने के लिए आर्रेनियस की परिभाषा व अनुसार अम्लों एवं क्षारवेफां के आयनन की विवेचना उपयोगी होगी। परक्लोरिक हाइड्रोक्लोरिक अम्ल (HCI) हाइड्रोब्रोमिक अम्ल (HBr) हाइड्रोआयोडिक अम्ल (HI) नाइट्रिक अम्ल एवं सल्फ्रयूरिक अम्ल आदि अम्लप्रबल’ कहलाते हैं, क्योंकि यह जलीय माध्यम में संगत आयनोंमें लगभग पूर्णतः वियोजित होकर प्रोटानदाता के समान कार्यकरते हैं। इसी प्रकार लीथियम हाइड्राक्साइड (LiOH) सोडियमहाइड्राक्साइड (NaOH), पोटैशियम हाइड्राक्साइड (KOH) सीशियम हाइड्राक्साइड (CsOH) एवं बेरियम हाइड्राक्साइड जलीय माध्यम में संगत आयनों में लगभग पूर्णतवियोजित होकर तथा आयन देते है
आरेनियस के सिद्धांत अनुसार, ये प्रबल क्षारक हैं, क्योंकि ये माध्यम में पूर्णतः वियोजित होकर क्रमशः आयन प्रदान करते हैं।विकल्पतः अम्ल या क्षार का सामथ्र्य अम्लों एवं क्षारकों के ब्रन्स्टेदलौरी सिद्धांत के अनुसार मापा जा सकता है। इसके अनुसार, ‘प्रबल अम्ल’ से तात्पर्य ‘एक उत्तम प्रोटानदाता’ एवंप्रबल क्षारक से तात्पर्य ‘उत्तम प्रोटानग्राही’ है।
दुर्बल अम्ल HAके अम्ल–क्षार वियोजन साम्य परविचार करें–
pH स्केल
हाइड्रोनियम आयन की मोलरता में सांद्रता को एक लघुगुणकीयमापक्रम (Logarthmic Scale) में सरलता से प्रदर्शित कियाजाता है, जिसे pH स्केल कहा जाता है।

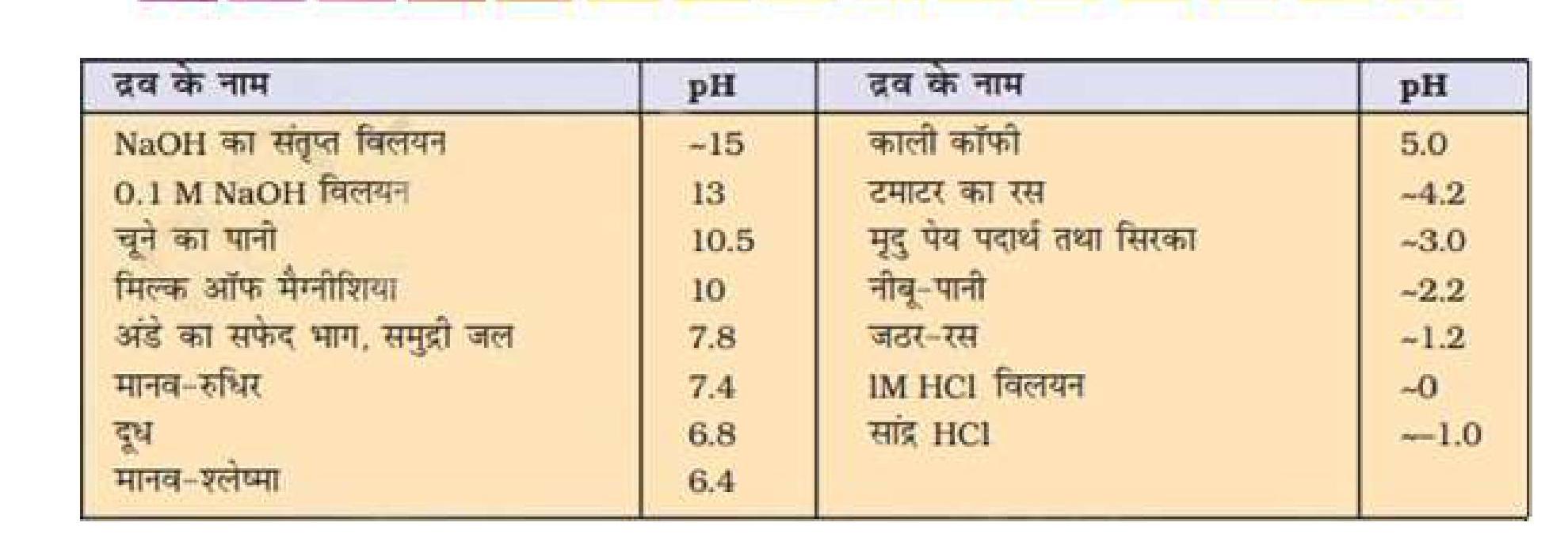
कुछ सामान्य पदार्थों की pHके मान
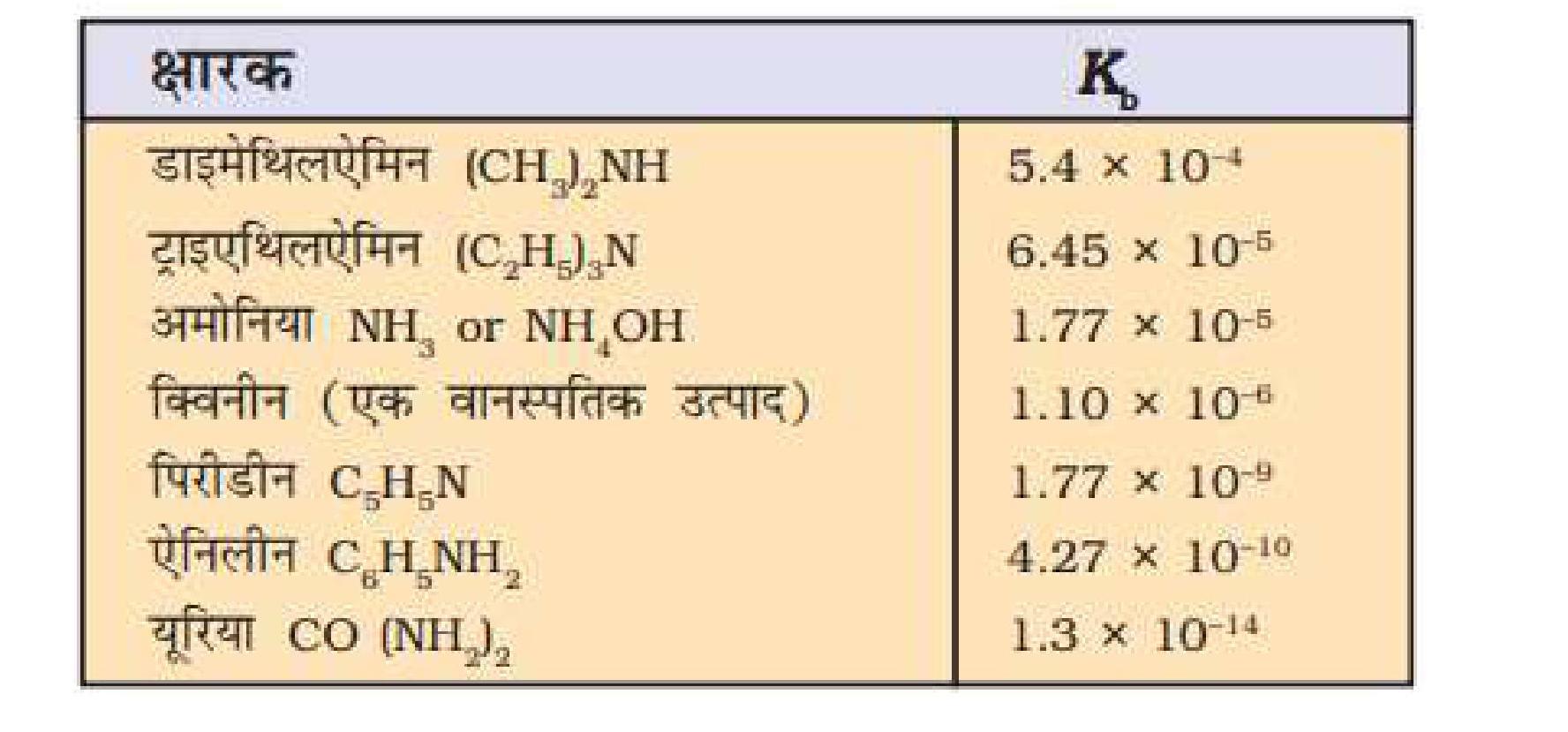
298K पर कुछ दुर्बल क्षारकों के आयनन–स्थिरांकके मान
Ka तथा Kb तथा में संबंध्
Ka तथा Kb क्रमशः अम्ल और क्षारक की सामथ्र्य को दर्शाते हैं। संयुग्मी अम्ल-क्षार युग्म में ये एक-दूसरे से सरलतम रूप से संबंध्ति होते हैं। यदि एक का मान ज्ञात है, तो दूसरे को ज्ञात किया जा सकता है। तथा के उदाहरण की विवेचना करते हैं।